Dendritic cells, FcγR, Inflammatory response, Innate immunity, Signal transduction, Lipid mediators
Teléfono: +34-983-423-273 (Despacho) Teléfono: +34-983-184-835 (Laboratorio)
e-mail: mscres@ibgm.uva.es
Nuestro trabajo abarca los mecanismos moleculares implicados en el desarrollo de daño tisular por mecanismo inmune y la caracterización de los principales mediadores químicos que se generan tras la ocupación de los receptores para los patrones moleculares asociados a patógenos y de los receptores para la porción Fc de los anticuerpos de la clase IgG. La cooperación entre estos receptores explica los modelos actuales de funcionamiento del sistema inmune, según los cuales ligandos escasamente solubles y particulados son los desencadenantes de la reacción inflamatoria aguda y de la iniciación de la respuesta adaptativa. Estos hechos son extraordinariamente relevantes para entender la patogenia de las enfermedades autoinmunes y la defensa frente a la invasión microbiana.
Hallazgos recientes de este laboratorio han sido:
Este hecho posee relevancia fisiológica puesto que el peptidoglicano es un componente mayoritario de la pared celular de bacterias Gram + y los polímeros de manosa (mannanos) son el componente fundamental de la porción externa de la pared celular de los hongos, lo que confiere a esto compuestos un papel relevante como patrones moleculares asociados a patógenos. La respuesta de los polimorfonucleares a estos ligandos fue comparable a la de los agonistas con mayor relevancia fisiopatológica actualmente conocidos como las partículas de zymosan revestidas de complemento y los inmunocomplejos de IgG.
Por el contrario, el ácido lipoteicoico, LPS, muramildipéptido y el análogo de lipoproteínas bacterianas palmitoil-3-cisteína-serina-lisina-4 (Pam3CSK4) no mostraron ningún efecto. La liberación de ácido araquidónico se acompañó de la producción de leucotrieno B4 y PGE2, lo que sugiere que las rutas de lipoxigenasas y ciclooxigenasas son activas en los polimorfonucleares humanos en respuesta a los patrones moleculares asociados a patógenos. El análisis de los extractos lipídicos de los sobrenadantes y de los pellets celulares y estudios farmacológicos con el inhibidor de calpaína calpeptin y el inhibidor de la fosfolipasa A2 citosólica pyrrolidina-1, mostraron la dependencia de la liberación de ácido araquidónico de reacciones catalizadas por la fosfolipasa A2 citosólica. El efecto del peptidoglicano no se pudo inhibir por le tratamiento previo con un anticuerpo TLR2 mAb, lo que sugiere, bien la ausencia de participación de este receptor, bien la cooperación necesaria de otros receptores.
Redes extracelulares de DNA en PMN expuestos a peptidoglicano de
S. aureus. El panel izquierdo muestra los núcleos de células control teñidas con DAPI. El panel derecho muestra PMN tratadas durante tres horas con 30 μg/ml de peptidoglicano en los que la estructura de la cromatina se ha distorsionado para formar las redes extracelulares.
- vi) El mecanismo de inducción de la proteína ciclooxigenasa-2 (COX-2) en polimorfonucleares humanos por los patrones moleculares asociados a patógenos. En este sistema, el peptidoglicano y el mannan, y en menor escala el homólogo de lipoproteínas bacterianas Pam3CSK4, indujeron la expresión de la proteína COX-2. Por el contrario, el ácido lipoteicoico y el muramildipeptido fueron estímulos irrelevantes. El mRNA que codifica la COX-2 estaba presente en los polimorfonucleares en estado basal en niveles similares a los detectados en células estimuladas, mientras que la detección de la proteína era indetectable. El tratamiento con el inhibidor de la fosfatidilinositol-3-kinasa (PI3K) wortmaninn, el inhibidor de mTOR (mammalian target of rapamycin) rapamycin y el inhibidor de la traducción cycloheximida bloqueó la inducción de la proteina COX-2 en respuesta a mannan y peptidoglicano, mientras que el inhibidor de la transcripción actinomycin D no mostró ningún efecto. Estos resultados han puesto de manifiesto la capacidad de los patrones moleculares asociados a patógenos para inducir el metabolismo oxidativo del ácido araquidónico de forma más robusta que los quimiotrayentes clásicos de polimorfonucleares, puesto que el mannan y el peptidoglicano hacen coincidir la liberación de ácido araquidónico con la rápida inducción de la proteína COX-2, regulada por una cascada de señalización que incluye PI3K, mTOR, y la maquinaria de traducción. Este mecanismo de inducción de la expresión de la proteína COX-2 en PMN es sustancialmente diferente del que se produce en fagocitos mononucleares, que depende, fundamentalmente, de la regulación transcripcional.
Secuencia de la porción 5’-UTR de COX-2. La secuencia y la estructura secundaria predicha de la porción 5’-UTR de COX-2 calculada usando RNAfold software, junto a los tractos de polipirimidinas subrayados en la secuencia se muestran en (A). Electroforesis en gel de agarosa de los productos de RT-PCR con el RNA obtenido de PMN en reposo utilizando distintas combinaciones de primers (B). Los diagramas de bandas muestran la localización de los primers usados en las reacciones y las calles se han marcado de acuerdo con las combinaciones de primers seleccionados para cada reacción.
- vii) La caracterización de los mecanismos moleculares que explican las distintas respuestas de las células dendríticas derivadas de monocitos a los patrones moleculares derivados de hongos que contienen manosa y polímeros de β-glucanos. Esta respuesta se caracteriza por la prominente inducción de COX-2, la alta producción de IL-10 e IL-23 y una reducida biosíntesis de IL-12 p70. La unión cooperativa de dectin-1 por β-glucanos y de DC-SIGN por le componente de manosa parece crucial para la inducción de estas respuestas.
The
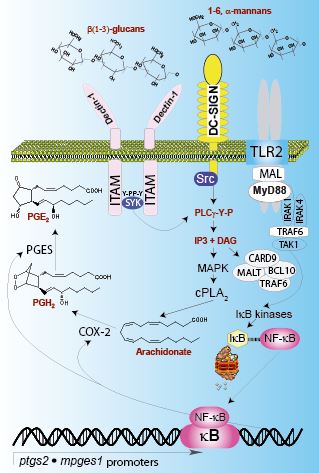
Candida paradigm for AA metabolism in DC. The mannan and β-glucan components of the fungal cell wall are recognized by at least DC-SIGN, TLR2, dectin-1, the mannose receptor, and dectin-2. This gives rise to a series of signalling events implicating activation of SYK and Src families of tyrosine kinases. Both routes converge to activate phospholipases Cγ and through the generation of diacylglycerol activate protein kinase C and MAPK cascades. Phosphorylation by MAPK and Ca
2+-driven translocation of cPLA
2α explain AA release from cell phospholipids. Activation of IκB kinases via MyD88 is a major factor explaining COX-2 and PGES induction. The CARD9/MALT/BCL10/TRAF6 complex is also involved in the activation of IκB kinases. DAG, diacylglycerol; IP
3, inositol 1,4,5-trisphosphate; IκB, inhibitory subunit of NF-κB; IRAK, interleukin-1 receptor-associated kinase; MAL, MyD88 adaptor-like; MAPK, mitogen-activated protein kinases; MyD88, myeloid differentiation primary response gene 88; PLCγ, phospholipase Cγ; P-Y, phosphotyrosine;
ptgs2, COX-2 gene;
mpges1, microsomal prostaglandin E synthase-1 gene; TAK1, transforming growth factor-β-activated kinase-1; TRAF6, TNF receptor-associated factor-6. This scheme has been constructed from the results reported by Valera et al. (
J Immunol180: 5727-5736. 2008), Suram et al. (
J Biol Chem281: 5506-5514, 2006 &
J Biol Chem285: 30676-30685, 2010), and Parti et al. (
Am J Respir Crit Care Med42: 415-423, 2011).
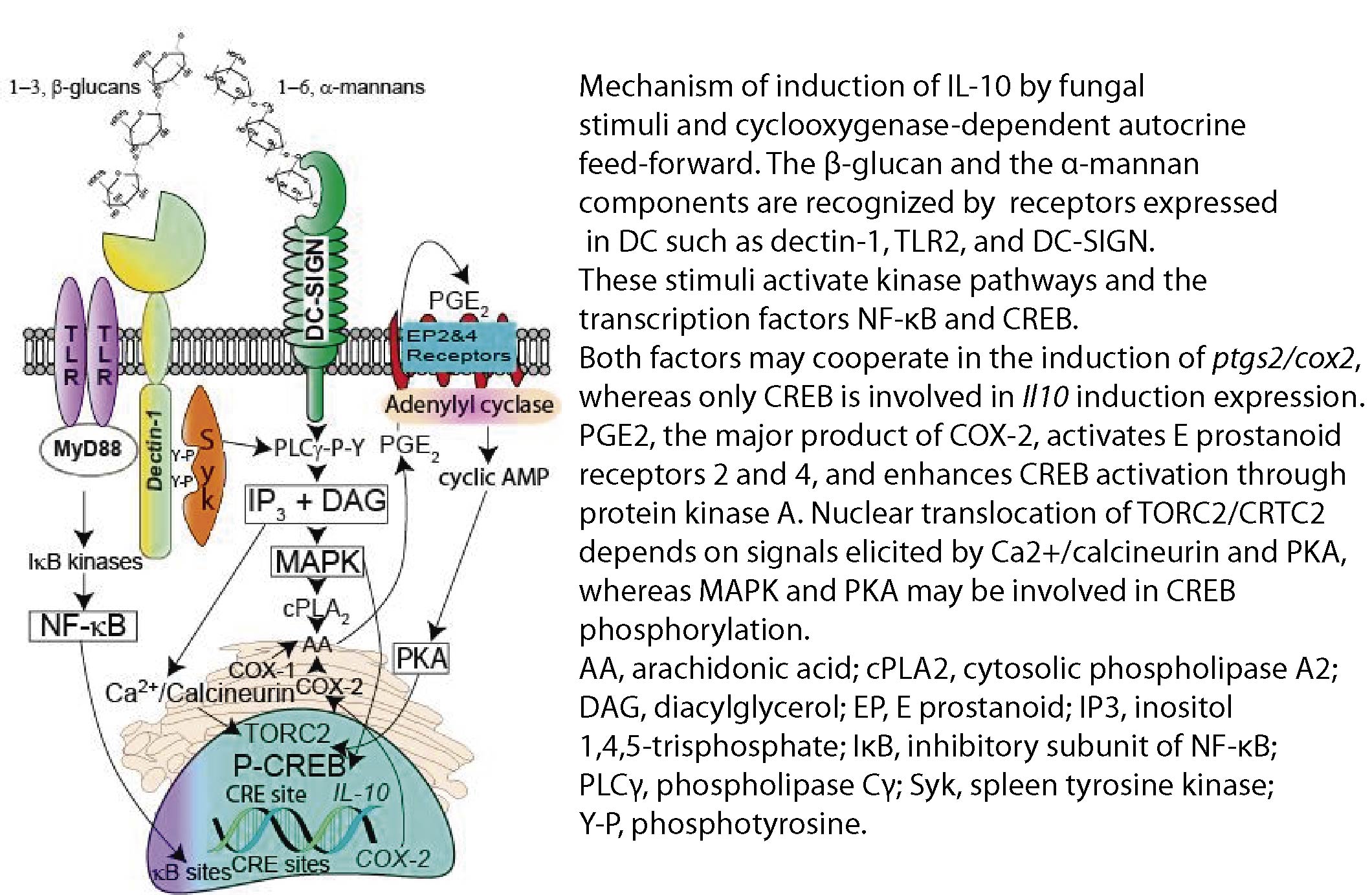
La alta producción de IL-10 asociada a la baja producción de IL-12 p70 puede explicarse por un mecanismo que implica la secreción autocrina de PGE2 y una red de interacciones entre PKA, MAP/ERK, (GSK3β) glicógeno sintasa kinasa-3β y calcineurina que regulan la actividad transcripcional de CREB (CRE binding protein) mediante su capacidad para unir los coactivadores CBP (CREB-binding protein) y CRTC2 (CREB regulated transcription coactivator, también denominado TORC2, transducer of regulated CREB activity) y disminuir la cantidad de CBP disponible para la interacción con otros factores de transcripción.
La investigación actual se dirige al análisis de las vías de señalización acopladas a la activación de los receptores del sistema inmune innato expresados en la superficie de las células dendríticas y a la caracterización de los mecanismos de regulación de la producción de citocinas que influyen en al polarización de la respuesta inmune hacia los tipos Th1, Th2 y Th17. En este sentido, recientemente hemos definido:
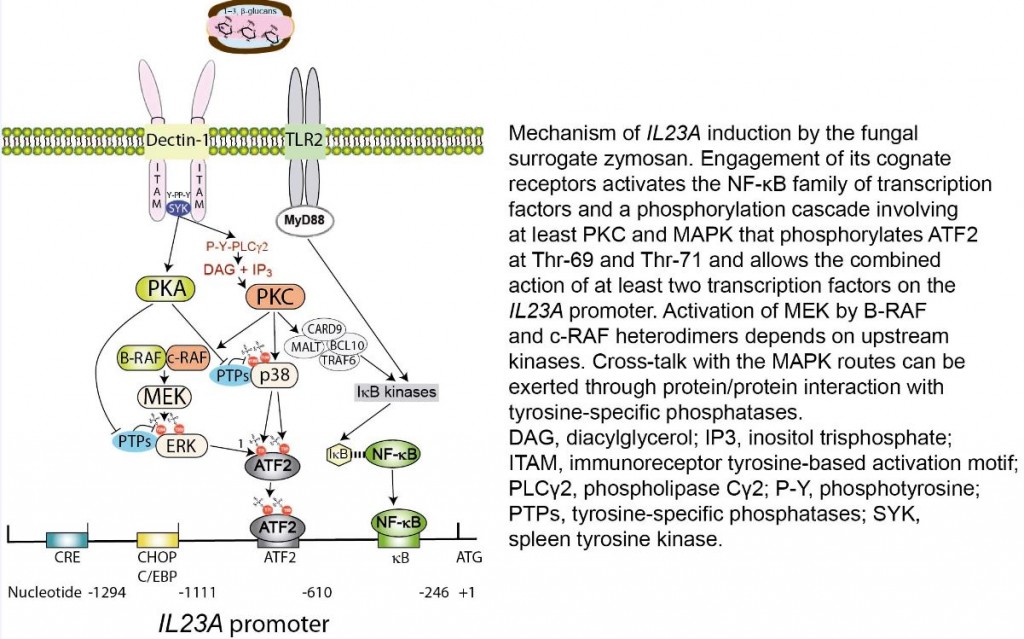
- El mecanismo de regulación transcripcional de IL23A (gen que codifica la cadena p19 de la citocina IL-23) mediante fosforilaciones complementarias del factor ATF.
2. La activación de SIRT1 durante la fagocitosis de patrones moleculares de la pared de hongos y su contribución a la represión de la transcripción de la cadena p35 de la citocina IL-12 p70.
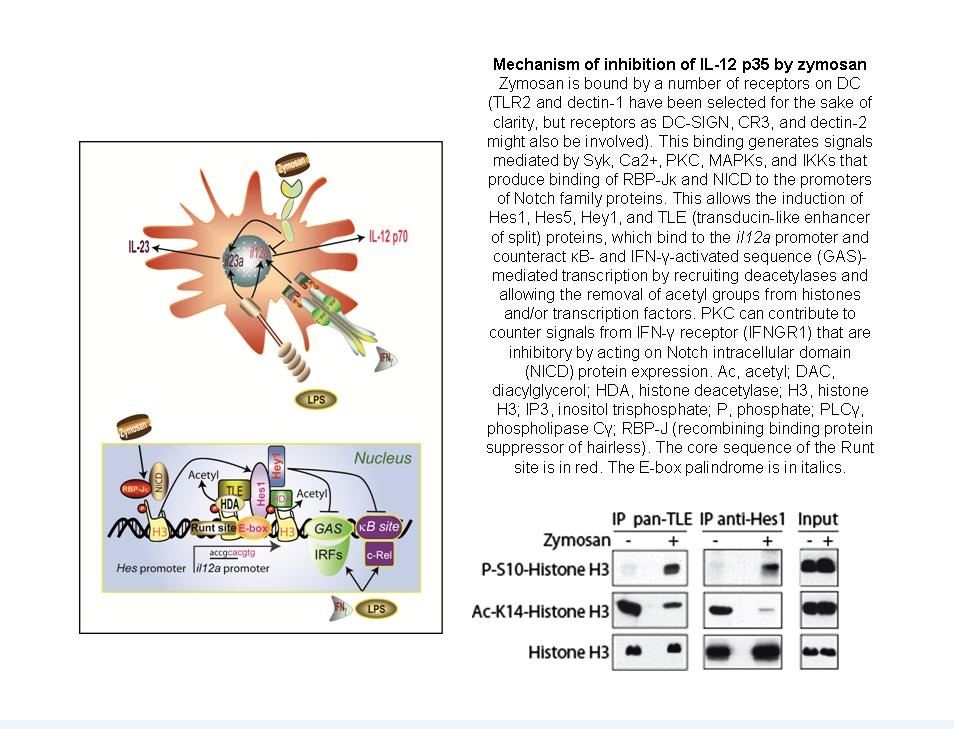
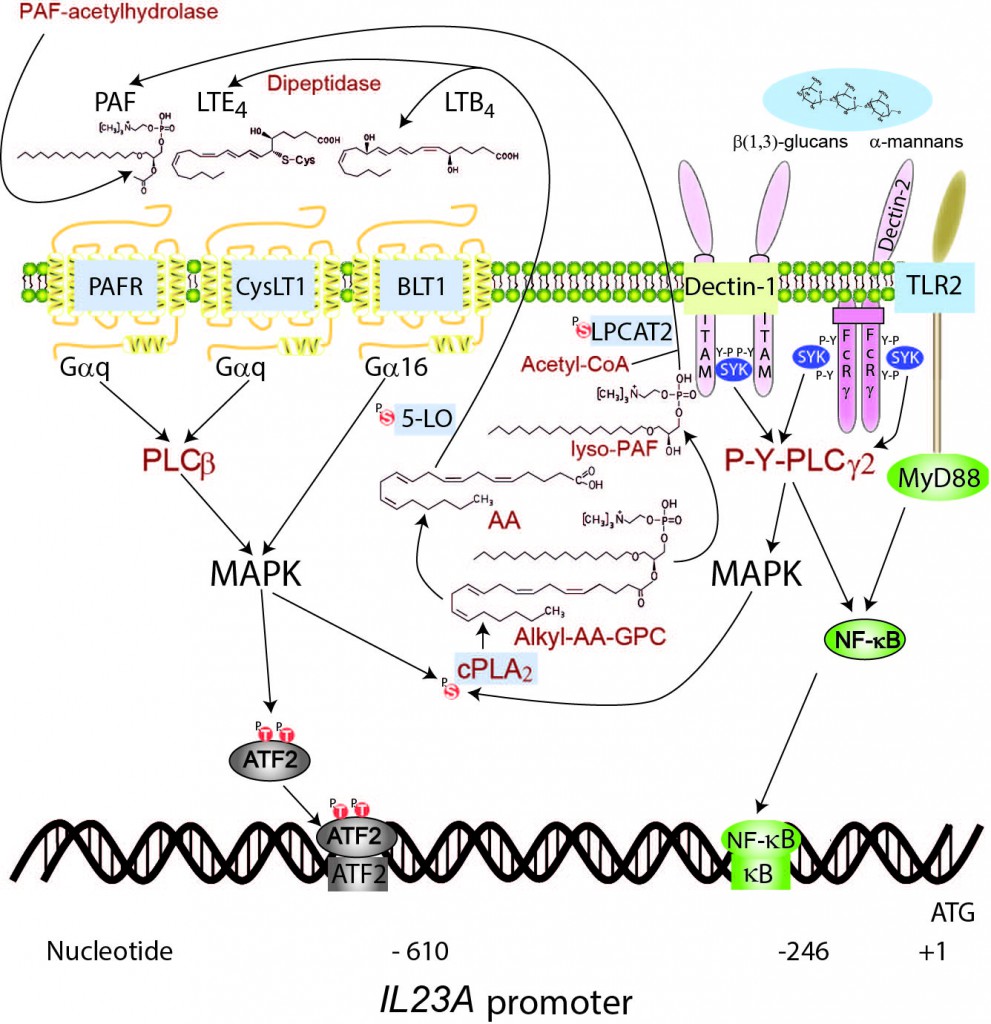 Cooperation of autocrine lipid mediators with fungal patterns to induce ATF2 phosphorylation and the trans-activation of IL23A through complementary phosphorylations of activating transcription factor 2 (ATF2). Fungal patterns activate the NF-κB family of transcription factors and a phosphorylation cascade involving at least PKC and MAPK that phosphorylates ATF2 at Thr69 and Thr71, cPLA2 at Ser505, 5-LO at Ser663, and LPCAT at Ser34. P-Ser505-cPLA2 hydrolyses 1-hexadecyl-2-arachidonoyl-sn-glycero-3-phosphocholine (hexadecyl-AA-GPC) and generates both free AA and 1-hexadecyl-2-lyso-glycero-3-phosphocholine (lyso-PAF) that by the action of 5-LO and LPCAT1/2 give rise to LTB4, cysteinyl-LT, and PAF. The lipid mediators activate another signaling cascade that further enhances their biosynthesis and the phosphorylation of ATF2. The combined action of NF-kB and ATF2 on the IL23A promoter allows its trans-activation. FcRγ, Fc receptor γ-chain; ITAM, immunoreceptor tyrosine-based activation motif; PLCβ, phospholipase Cβ; PLCγ2, phospholipase Cγ2; P, phosphate; P-Y, phosphotyrosine; SYK, spleen tyrosine kinase; TLR2, Toll-like receptor 2.
Cooperation of autocrine lipid mediators with fungal patterns to induce ATF2 phosphorylation and the trans-activation of IL23A through complementary phosphorylations of activating transcription factor 2 (ATF2). Fungal patterns activate the NF-κB family of transcription factors and a phosphorylation cascade involving at least PKC and MAPK that phosphorylates ATF2 at Thr69 and Thr71, cPLA2 at Ser505, 5-LO at Ser663, and LPCAT at Ser34. P-Ser505-cPLA2 hydrolyses 1-hexadecyl-2-arachidonoyl-sn-glycero-3-phosphocholine (hexadecyl-AA-GPC) and generates both free AA and 1-hexadecyl-2-lyso-glycero-3-phosphocholine (lyso-PAF) that by the action of 5-LO and LPCAT1/2 give rise to LTB4, cysteinyl-LT, and PAF. The lipid mediators activate another signaling cascade that further enhances their biosynthesis and the phosphorylation of ATF2. The combined action of NF-kB and ATF2 on the IL23A promoter allows its trans-activation. FcRγ, Fc receptor γ-chain; ITAM, immunoreceptor tyrosine-based activation motif; PLCβ, phospholipase Cβ; PLCγ2, phospholipase Cγ2; P, phosphate; P-Y, phosphotyrosine; SYK, spleen tyrosine kinase; TLR2, Toll-like receptor 2.
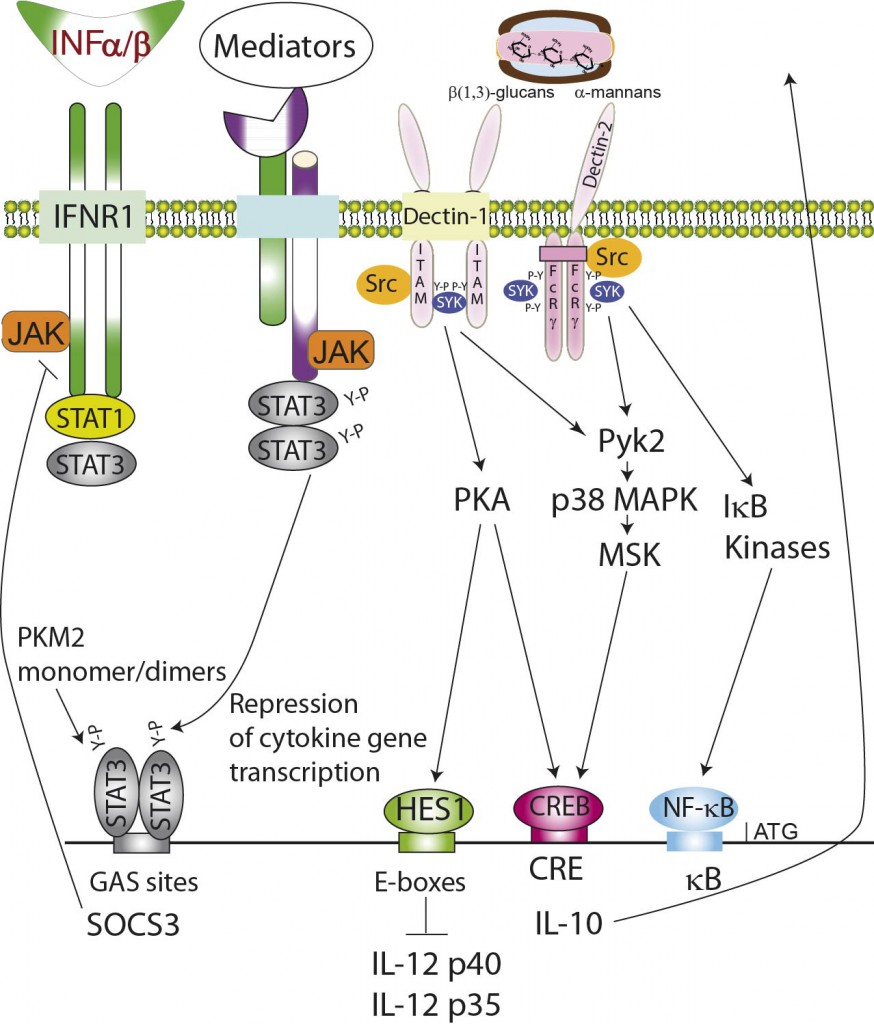
Binding of α-mannan and β-glucan moieties initiates a series of phosphorylation reactions involving MAP kinases, protein kinase A, IkB kinases, as well as nuclear monomer/dimers of the key metabolic regulator pyruvate kinase M2 (PKM2).1 The activation of the latent cytoplasmic transcription factors CREB and NF-kB trans-activates the IL-10 and IL-12 family cytokine promoters. The concomitant activation of repressors of the NOTCH family, for instance HES1,2-4 contributes to blunt the production of IL-12 p70 protein. A network of secondary mediators activates the formation of Y705-STAT3 dimers that both directly and through the transcriptional activation of SOCS genes contribute to the repression of cytokine gene transcription.
El objetivo final de nuestra investigación es la caracterización de los receptores celulares y de las vías de señalización que pueden constituir dianas farmacológicas relevantes para el tratamiento de enfermedades autoinmunes, glomerulonefritis, vasculitis y enfermedades pulmonares de base inflamatoria.
 The Candida paradigm for AA metabolism in DC. The mannan and β-glucan components of the fungal cell wall are recognized by at least DC-SIGN, TLR2, dectin-1, the mannose receptor, and dectin-2. This gives rise to a series of signalling events implicating activation of SYK and Src families of tyrosine kinases. Both routes converge to activate phospholipases Cγ and through the generation of diacylglycerol activate protein kinase C and MAPK cascades. Phosphorylation by MAPK and Ca2+-driven translocation of cPLA2α explain AA release from cell phospholipids. Activation of IκB kinases via MyD88 is a major factor explaining COX-2 and PGES induction. The CARD9/MALT/BCL10/TRAF6 complex is also involved in the activation of IκB kinases. DAG, diacylglycerol; IP3, inositol 1,4,5-trisphosphate; IκB, inhibitory subunit of NF-κB; IRAK, interleukin-1 receptor-associated kinase; MAL, MyD88 adaptor-like; MAPK, mitogen-activated protein kinases; MyD88, myeloid differentiation primary response gene 88; PLCγ, phospholipase Cγ; P-Y, phosphotyrosine; ptgs2, COX-2 gene; mpges1, microsomal prostaglandin E synthase-1 gene; TAK1, transforming growth factor-β-activated kinase-1; TRAF6, TNF receptor-associated factor-6. This scheme has been constructed from the results reported by Valera et al. (J Immunol180: 5727-5736. 2008), Suram et al. (J Biol Chem281: 5506-5514, 2006 & J Biol Chem285: 30676-30685, 2010), and Parti et al. (Am J Respir Crit Care Med42: 415-423, 2011).
La alta producción de IL-10 asociada a la baja producción de IL-12 p70 puede explicarse por un mecanismo que implica la secreción autocrina de PGE2 y una red de interacciones entre PKA, MAP/ERK, (GSK3β) glicógeno sintasa kinasa-3β y calcineurina que regulan la actividad transcripcional de CREB (CRE binding protein) mediante su capacidad para unir los coactivadores CBP (CREB-binding protein) y CRTC2 (CREB regulated transcription coactivator, también denominado TORC2, transducer of regulated CREB activity) y disminuir la cantidad de CBP disponible para la interacción con otros factores de transcripción.
The Candida paradigm for AA metabolism in DC. The mannan and β-glucan components of the fungal cell wall are recognized by at least DC-SIGN, TLR2, dectin-1, the mannose receptor, and dectin-2. This gives rise to a series of signalling events implicating activation of SYK and Src families of tyrosine kinases. Both routes converge to activate phospholipases Cγ and through the generation of diacylglycerol activate protein kinase C and MAPK cascades. Phosphorylation by MAPK and Ca2+-driven translocation of cPLA2α explain AA release from cell phospholipids. Activation of IκB kinases via MyD88 is a major factor explaining COX-2 and PGES induction. The CARD9/MALT/BCL10/TRAF6 complex is also involved in the activation of IκB kinases. DAG, diacylglycerol; IP3, inositol 1,4,5-trisphosphate; IκB, inhibitory subunit of NF-κB; IRAK, interleukin-1 receptor-associated kinase; MAL, MyD88 adaptor-like; MAPK, mitogen-activated protein kinases; MyD88, myeloid differentiation primary response gene 88; PLCγ, phospholipase Cγ; P-Y, phosphotyrosine; ptgs2, COX-2 gene; mpges1, microsomal prostaglandin E synthase-1 gene; TAK1, transforming growth factor-β-activated kinase-1; TRAF6, TNF receptor-associated factor-6. This scheme has been constructed from the results reported by Valera et al. (J Immunol180: 5727-5736. 2008), Suram et al. (J Biol Chem281: 5506-5514, 2006 & J Biol Chem285: 30676-30685, 2010), and Parti et al. (Am J Respir Crit Care Med42: 415-423, 2011).
La alta producción de IL-10 asociada a la baja producción de IL-12 p70 puede explicarse por un mecanismo que implica la secreción autocrina de PGE2 y una red de interacciones entre PKA, MAP/ERK, (GSK3β) glicógeno sintasa kinasa-3β y calcineurina que regulan la actividad transcripcional de CREB (CRE binding protein) mediante su capacidad para unir los coactivadores CBP (CREB-binding protein) y CRTC2 (CREB regulated transcription coactivator, también denominado TORC2, transducer of regulated CREB activity) y disminuir la cantidad de CBP disponible para la interacción con otros factores de transcripción.
 La investigación actual se dirige al análisis de las vías de señalización acopladas a la activación de los receptores del sistema inmune innato expresados en la superficie de las células dendríticas y a la caracterización de los mecanismos de regulación de la producción de citocinas que influyen en al polarización de la respuesta inmune hacia los tipos Th1, Th2 y Th17. En este sentido, recientemente hemos definido:
La investigación actual se dirige al análisis de las vías de señalización acopladas a la activación de los receptores del sistema inmune innato expresados en la superficie de las células dendríticas y a la caracterización de los mecanismos de regulación de la producción de citocinas que influyen en al polarización de la respuesta inmune hacia los tipos Th1, Th2 y Th17. En este sentido, recientemente hemos definido:
 2. La activación de SIRT1 durante la fagocitosis de patrones moleculares de la pared de hongos y su contribución a la represión de la transcripción de la cadena p35 de la citocina IL-12 p70.
2. La activación de SIRT1 durante la fagocitosis de patrones moleculares de la pared de hongos y su contribución a la represión de la transcripción de la cadena p35 de la citocina IL-12 p70.

 Cooperation of autocrine lipid mediators with fungal patterns to induce ATF2 phosphorylation and the trans-activation of IL23A through complementary phosphorylations of activating transcription factor 2 (ATF2). Fungal patterns activate the NF-κB family of transcription factors and a phosphorylation cascade involving at least PKC and MAPK that phosphorylates ATF2 at Thr69 and Thr71, cPLA2 at Ser505, 5-LO at Ser663, and LPCAT at Ser34. P-Ser505-cPLA2 hydrolyses 1-hexadecyl-2-arachidonoyl-sn-glycero-3-phosphocholine (hexadecyl-AA-GPC) and generates both free AA and 1-hexadecyl-2-lyso-glycero-3-phosphocholine (lyso-PAF) that by the action of 5-LO and LPCAT1/2 give rise to LTB4, cysteinyl-LT, and PAF. The lipid mediators activate another signaling cascade that further enhances their biosynthesis and the phosphorylation of ATF2. The combined action of NF-kB and ATF2 on the IL23A promoter allows its trans-activation. FcRγ, Fc receptor γ-chain; ITAM, immunoreceptor tyrosine-based activation motif; PLCβ, phospholipase Cβ; PLCγ2, phospholipase Cγ2; P, phosphate; P-Y, phosphotyrosine; SYK, spleen tyrosine kinase; TLR2, Toll-like receptor 2.
Cooperation of autocrine lipid mediators with fungal patterns to induce ATF2 phosphorylation and the trans-activation of IL23A through complementary phosphorylations of activating transcription factor 2 (ATF2). Fungal patterns activate the NF-κB family of transcription factors and a phosphorylation cascade involving at least PKC and MAPK that phosphorylates ATF2 at Thr69 and Thr71, cPLA2 at Ser505, 5-LO at Ser663, and LPCAT at Ser34. P-Ser505-cPLA2 hydrolyses 1-hexadecyl-2-arachidonoyl-sn-glycero-3-phosphocholine (hexadecyl-AA-GPC) and generates both free AA and 1-hexadecyl-2-lyso-glycero-3-phosphocholine (lyso-PAF) that by the action of 5-LO and LPCAT1/2 give rise to LTB4, cysteinyl-LT, and PAF. The lipid mediators activate another signaling cascade that further enhances their biosynthesis and the phosphorylation of ATF2. The combined action of NF-kB and ATF2 on the IL23A promoter allows its trans-activation. FcRγ, Fc receptor γ-chain; ITAM, immunoreceptor tyrosine-based activation motif; PLCβ, phospholipase Cβ; PLCγ2, phospholipase Cγ2; P, phosphate; P-Y, phosphotyrosine; SYK, spleen tyrosine kinase; TLR2, Toll-like receptor 2.
 El objetivo final de nuestra investigación es la caracterización de los receptores celulares y de las vías de señalización que pueden constituir dianas farmacológicas relevantes para el tratamiento de enfermedades autoinmunes, glomerulonefritis, vasculitis y enfermedades pulmonares de base inflamatoria.
El objetivo final de nuestra investigación es la caracterización de los receptores celulares y de las vías de señalización que pueden constituir dianas farmacológicas relevantes para el tratamiento de enfermedades autoinmunes, glomerulonefritis, vasculitis y enfermedades pulmonares de base inflamatoria.

